Sábado, 19 de abril de 2025 | Porto Velho (RO)
Sexta-feira, 26 de novembro de 2021 - 11h07

O molnupiravir, medicamento para combate à covid-19, teve o seu pedido
de uso emergencial apresentado, nesta sexta-feira (26), à Agência Nacional de
Vigilância Sanitária (Anvisa) pela empresa Merck Sharp & Dohme.
De acordo com a empresa, “estudos demonstram que o medicamento, quando
administrado no início da infecção, tem a capacidade de reduzir casos de hospitalização
e mortes", dados que serão revisados pela Anvisa.
“As primeiras 24 horas de análise serão utilizadas para fazer uma
triagem do processo e verificar se os documentos necessários estão disponíveis.
Se houver informação importante faltando, a Anvisa pode solicitar ao
laboratório”, informou a agência.
A Anvisa lembrou que o prazo de avaliação do uso emergencial e
temporário de medicamento é de até 30 dias. “A análise não considera o tempo do
processo em status de exigência técnica, que é quando o laboratório precisa
responder questões técnicas feitas pela agência dentro do processo”.
No dia 19 de novembro, a Anvisa e o laboratório já haviam realizado a
reunião de pré-submissão do produto, que ocorreu antes do envio formal do
pedido à Anvisa pela empresa.
 Sábado, 19 de abril de 2025 | Porto Velho (RO)
Sábado, 19 de abril de 2025 | Porto Velho (RO)
Ministério da Saúde retoma maior pesquisa sobre Covid no Brasil
A partir desta segunda-feira (11), pesquisadores a serviço do Ministério da Saúde darão início à coleta de dados para uma nova fase do maior estudo
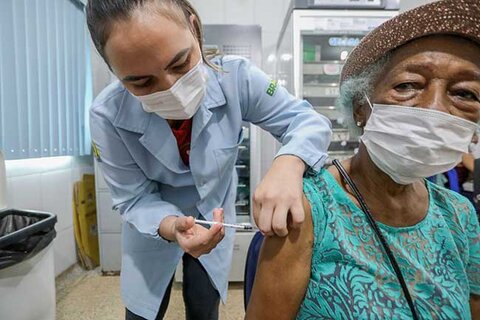
Vacina bivalente contra a covid-19 começou a ser aplicada em Porto Velho
A Prefeitura de Porto Velho, através da Secretaria Municipal de Saúde (Semusa), começou hoje a vacinação bivalente contra a covid-19 em idosos acima d
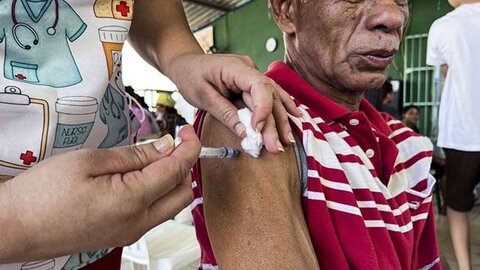
Porto Velho inicia vacinação bivalente para idosos a partir de 60 anos na segunda-feira (27)
A Prefeitura de Porto Velho, através da Secretaria Municipal de Saúde (Semusa), inicia na segunda-feira (27) a vacinação bivalente contra a covid-19
 Sábado, 19 de abril de 2025 | Porto Velho (RO)
Sábado, 19 de abril de 2025 | Porto Velho (RO)